В самом сердце химических элементов, скрытых в таблице Менделеева, находится тайна энергетических уровней. Эти невидимые миры, где частицы воздвигают невидимые стены и сила притяжения струится между ними – это то, что формирует химическую природу каждого элемента.
Взглянув с микроскопической точки зрения, энергетический уровень можно представить как некий "этаж" вокруг атомного ядра, на котором находятся электроны. Здесь, в мысленной панораме, электроны прыгают и вращаются, создавая наиболее выгодные электростатические конфигурации, чтобы достичь состояния минимальной потенциальной энергии.
Некоторые электроны находятся на самом низком уровне, практически опутанные витиеватыми "тропами" электростатических сил, которые удерживают их там. Но другие, обладая бОльшей энергией, поднимаются на более высокие уровни, почти свободно перемещаясь между ними, создавая разнообразные химические реакции и связи.
Определение понятия "энергетический уровень" в химии
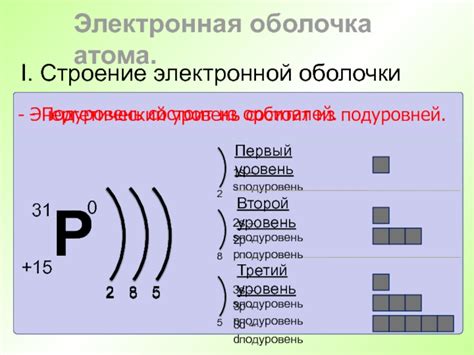
В химии существует важное понятие "энергетический уровень", которое играет ключевую роль в объяснении свойств и поведения атомов и молекул. Энергетический уровень описывает возможное состояние энергии, в котором находится частица, и ее квантовые свойства. Путем изучения энергетических уровней можно понять, как различные частицы реагируют на внешние воздействия и как они образуют и разрушают химические связи.
Каждый энергетический уровень обладает свойствами и характеризуется определенными значениями энергии. Они представляют собой дискретные значения энергии, которые атом или молекула могут иметь. Интересно то, что эти уровни называются "квантовыми", так как их значения ограничены определенными дискретными значениями, которые нельзя непрерывно изменять.
Квантовые значения энергетических уровней связаны с конкретными состояниями энергии, в которых могут находиться атомы и молекулы. Например, электроны в атоме располагаются на различных энергетических уровнях, и переход электрона с одного уровня на другой сопровождается поглощением или испусканием определенного количества энергии в виде света.
Изучение энергетических уровней позволяет химикам понять, как происходят химические реакции, почему определенные соединения устойчивы, а другие нет, и какие физические процессы и явления происходят на молекулярном уровне. Понимание энергетических уровней является фундаментальной основой в современной химии и имеет широкое применение в различных областях химической науки и технологии.
Структура и организация таблицы периодических элементов в химии

Данная таблица является основополагающим инструментом для химиков, ведь именно в ней содержится информация о строении атома, его энергетической структуре и других важных свойствах элементов. Таблица Менделеева представляет собой уникальную схему, в которой каждый элемент расположен в определенных строках и столбцах в соответствии с их атомными свойствами и химическими характеристиками.
Разработанная в XIX веке русским химиком Дмитрием Ивановичем Менделеевым, таблица Менделеева играет фундаментальную роль в организации и систематизации информации о химических элементах, позволяя увидеть их общие закономерности и периодические свойства.
Структура таблицы Менделеева включает в себя периоды – горизонтальные ряды, представляющие собой последовательность атомных чисел элементов. Периоды расположены от первого до седьмого и характеризуют изменение главного энергетического уровня атома по мере движения слева направо. Строки и столбцы таблицы Менделеева также отражают группы элементов, имеющих схожую строение внешней электронной оболочки и химические свойства. Упорядочение элементов по группам позволяет установить связь между их внутренней структурой и превалирующими ионными и химическими свойствами.
Связь местоположения элементов в таблице Менделеева с их энергетическими уровнями

Когда мы рассматриваем таблицу Менделеева, мы можем заметить, что расположение элементов в ней имеет глубокую связь с их энергетическими уровнями. Энергетические уровни указывают на количество энергии, необходимой для атома или иона, чтобы находиться в определенном состоянии. Позиция элемента в таблице Менделеева отражает его энергетические свойства и его распределение в энергетических уровнях.
Верхние строки таблицы: На верхних строках таблицы Менделеева находятся элементы с наибольшим количеством энергетических уровней. Это говорит о том, что эти элементы имеют больше энергии, что позволяет им находиться в различных состояниях, обладать разнообразными свойствами и формировать большее количество химических соединений.
Последовательное увеличение энергетических уровней: Когда движемся вниз по таблице Менделеева, количество энергетических уровней в элементах увеличивается. Это показывает, что элементы, находящиеся ниже, имеют больше энергии, что расширяет возможности для образования соединений и проявления разнообразных химических свойств.
Блоки и группы элементов: Расположение элементов внутри блоков и групп также участвует в формировании энергетических уровней. Элементы одного блока обладают похожими энергетическими свойствами, так как находятся на одном энергетическом уровне. Группы элементов в одной группе имеют схожие энергетические уровни, что позволяет им демонстрировать сходные химические свойства.
Таким образом, расположение элементов в таблице Менделеева является не случайным, а имеет глубокую связь с их энергетическими уровнями. Это позволяет ученым изучать и предсказывать химические свойства элементов, а также создавать новые соединения и материалы на основе энергетических закономерностей.
Определение энергетического уровня элемента

Изучение химических свойств элементов включает понятие энергетического уровня, который определяет поведение атомов и молекул в химических реакциях. Такой уровень можно рассматривать как энергетическую "ступеньку", на которой находятся атомы в процессе изменения своего состояния. Как определить этот уровень в контексте таблицы Менделеева?
Для определения энергетического уровня элемента в таблице Менделеева используются его электронные конфигурации, где отображено распределение электронов по энергетическим орбиталям. Каждый электрон занимает определенную орбиталь, которая имеет определенную энергию. Чем дальше от ядра находится орбиталь, тем выше энергетический уровень электрона.
В таблице Менделеева можно увидеть, что элементы расположены по возрастанию атомного номера. Соответственно, с увеличением атомного номера увеличивается и количество электронов в атоме. Каждый новый электрон сначала заполняет орбиталь на более низком энергетическом уровне, а затем переходит на более высокий энергетический уровень.
Энергетические уровни элементов можно представить как "этажи" в строении атома. Каждый энергетический уровень может вмещать только определенное количество электронов, и в случае заполнения всех уровней, атом считается стабильным и малоактивным химически.
Таким образом, для определения энергетического уровня элемента в таблице Менделеева необходимо изучить его электронную конфигурацию и определить, на каких орбиталях находятся электроны и на каких уровнях эти орбитали расположены.
Факторы, определяющие энергетический уровень элемента

Каждый химический элемент обладает своим уникальным энергетическим уровнем, который определяет его химические свойства и поведение. Различные факторы влияют на энергетический уровень элемента, включая его атомную структуру, электронную конфигурацию и взаимодействие с окружающими частицами.
Атомы элементов обладают различными энергетическими уровнями электронов, которые можно представить как размещение электронов на "энергетических лестницах". Каждый энергетический уровень соответствует определенной энергии электрона, и он уникален для каждого элемента. Количество энергетических уровней, а также их расположение, зависит от количества электронов в атоме.
Одним из важных факторов, влияющих на энергетический уровень элемента, является его электронная конфигурация. Электроны могут находиться на различных энергетических уровнях, расположенных вокруг ядра атома. Число электронов на каждом энергетическом уровне определяет электронную конфигурацию элемента. Электронная конфигурация влияет на энергетический уровень элемента, а значит и на его свойства и реактивность.
Кроме того, взаимодействие элемента с окружающими атомами и молекулами также оказывает влияние на его энергетический уровень. Химические связи, образуемые между элементами, могут приводить к перераспределению энергии электронов и изменению их энергетического уровня. Взаимодействие с окружающими частицами может изменять энергетический уровень элемента как в положительную, так и в отрицательную сторону.
| Факторы, влияющие на энергетический уровень элемента: |
|---|
| Атомная структура |
| Электронная конфигурация |
| Взаимодействие с окружающими частицами |
Влияние энергетического уровня на характеристики элементов
Возможность атомов ионизироваться и образовывать соединения обусловлена их энергетическим уровнем, который определяет поведение элементов в химических реакциях и их физические свойства. Уровень энергии, динамически заряженный внутри атомов, формирует основу для понимания характеристик элементов и построения периодической системы.
Энергетический уровень влияет на способность атомов взаимодействовать с другими атомами и молекулами. Чем выше энергетический уровень, тем более активным будет атом, и он будет более склонным к реакциям с другими веществами. Напротив, нижние энергетические уровни могут свидетельствовать о большей стабильности атома и его менее активных свойствах.
Энергетический уровень также определяет расположение элементов в периодической таблице. Строка периодической таблицы соответствует уровням энергии электронов, прикрепленных к атомным ядрам. Чем ближе элемент находится к началу периода, тем меньше энергетический уровень этих электронов, что в свою очередь оказывает влияние на их свойства.
- Элементы с малыми энергетическими уровнями обычно имеют малую электроотрицательность, что делает их металлами.
- Элементы с более высокими энергетическими уровнями имеют более высокую электроотрицательность, что делает их неметаллами.
- Полуметаллы занимают промежуточное положение в периодической таблице, так как их энергетические уровни находятся между уровнями металлов и неметаллов.
Свойства элементов, такие как валентность, радиус атома, электронная конфигурация и т. д., тесно связаны с их энергетическими уровнями. Понимание этой связи помогает ученым классифицировать элементы и предсказывать их химическое и физическое поведение в различных условиях.
Значение энергетического уровня в химических реакциях

В химической науке существует понятие энергетического уровня, которое играет важную роль в химических реакциях. Этот уровень связан с процессами, связанными с переходом вещества из одного состояния в другое, такие как образование и разрушение связей между атомами и молекулами.
Энергетический уровень можно рассматривать как энергетическую платформу, на которой происходят реакции. На этом уровне атомы и молекулы могут находиться в различных энергетических состояниях, которые определяют их способность вступать в химические реакции. Более высокие энергетические уровни связаны с более нестабильными состояниями, где атомы и молекулы имеют больше энергии и склонность к реакциям, а более низкие уровни связаны с более стабильными состояниями.
Понимание энергетического уровня в химических реакциях позволяет ученым предсказывать и объяснять, какие реакции возможны и какие процессы протекают в химических системах. Энергия, связанная с уровнем, может быть поглощена или высвобождена во время химической реакции, что влияет на ее направленность и скорость.
Важно отметить, что энергетический уровень не связан с таблицей Менделеева, которая используется для классификации химических элементов. Таблица Менделеева представляет собой систематическое упорядочение элементов по их атомному номеру и химическим свойствам.
Исследования структуры энергетических уровней химических элементов
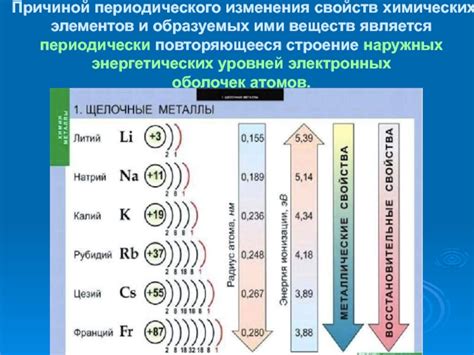
Энергетические уровни химических элементов представляют собой особую сферу исследований в области ядерной физики и химии. Понимание структуры этих уровней позволяет углубить наши знания о свойствах элементов и их взаимодействии с окружающей средой.
Исследования энергетических уровней редких элементов и обработка полученных данных вносят значительный вклад в развитие технологий и научных открытий. Они позволяют лучше понять особенности и характеристики определенных элементов, таких как трансурановые и радиоактивные.
- Данные исследований энергетических уровней помогают более точно определить периоды полураспада радиоактивных изотопов и предсказать их дальнейшую эволюцию.
- Изучение структуры энергетических уровней различных элементов позволяет лучше понять химические свойства и реакционную способность веществ.
- Результаты исследований помогают разрабатывать новые методы синтеза и получения химических элементов, что имеет применение в различных областях науки и техники.
- Исследования энергетических уровней элементов могут также применяться в медицине для разработки радиофармпрепаратов и диагностических методов.
Обширные исследования энергетических уровней химических элементов продолжаются и постоянно привлекают внимание ученых со всего мира. Это является важным пунктом в изучении структуры и свойств веществ, а также сырьевой базы для различных промышленных исследований и технологий.
Энергетические уровни и организация электронной структуры атомов

Энергетические уровни представляют собой конкретные значения энергии, на которых могут находиться электроны. Являясь своего рода "энергетическими этажами", эти уровни предлагают электронам определенные возможности и ограничения в их взаимодействии с другими атомами и построении химических связей.
- На самом низком энергетическом уровне, ближайшем к ядру, могут находиться только два электрона. Этот уровень называется 1s, где "s" обозначает форму орбитали этих электронов. Располагаясь на наименьшем расстоянии от ядра, эти электроны обладают наиболее высокой энергией среди электронов в атоме.
- Следующий по энергетическому уровню является 2s, где находятся еще два электрона. Затем идут уровни 2p, 3s, 3p, 4s и так далее, каждый из которых может содержать разное количество электронов в зависимости от сложности атома.
- Важно отметить, что каждый энергетический уровень имеет свою уникальную энергию, при которой электрон находится в состоянии наименьшей возможной энергии. При взаимодействии с другими атомами или внешними условиями, электроны могут переходить с одного уровня на другой, поглощая или испуская энергию в виде фотонов.
Понимание энергетических уровней и электронной структуры атомов является фундаментом для объяснения химических свойств элементов и основным инструментом в теории химических соединений. Систематическое изучение этих концепций позволяет получить представление о поведении атомов в различных условиях и строить модели веществ, а также прогнозировать их реакционную активность.
Вопрос-ответ

Что такое энергетический уровень в таблице Менделеева?
Энергетический уровень в таблице Менделеева - это один из ключевых параметров атома, который отражает энергию электронов, находящихся в атоме. Энергетическим уровнем обычно называют энергию, которую электрон должен иметь для того, чтобы находиться в определенной области вокруг атомного ядра.
Как количество энергетических уровней связано с электронной оболочкой атома?
Количество энергетических уровней в атоме определяет количество электронных оболочек, которые могут существовать в атоме. Каждая электронная оболочка соответствует определенному энергетическому уровню. Например, водородный атом имеет только один энергетический уровень и, соответственно, одну электронную оболочку.
Что определяет положение энергетических уровней в таблице Менделеева?
Положение энергетических уровней в таблице Менделеева определяется атомным номером элемента. Атомный номер представляет собой количество протонов в ядре атома и указывает на число электронов, находящихся на энергетических уровнях. Чем больше атомный номер элемента, тем выше находятся энергетические уровни в таблице Менделеева.
Какие свойства атома связаны с энергетическими уровнями?
Энергетические уровни атома определяют его химические свойства. Например, количество электронов на каждом энергетическом уровне определяет электронную конфигурацию атома и его возможность образовывать химические связи с другими атомами. Также энергетические уровни влияют на способность атома поглощать и испускать энергию в виде света или тепла.
Как энергетические уровни в таблице Менделеева связаны с периодами и группами элементов?
Электроны заполняют энергетические уровни в определенном порядке, начиная с ближайшего к ядру. Каждый период таблицы Менделеева соответствует новой электронной оболочке и, следовательно, новому энергетическому уровню. Группы элементов в таблице Менделеева имеют одинаковое количество электронов на своей внешней энергетической оболочке, что определяет их химические свойства.
Что такое энергетический уровень и как он связан с таблицей Менделеева?
Энергетический уровень – это энергетическая характеристика электронов в атоме, которая отображается в таблице Менделеева. Энергетические уровни разделены на шеллы и подшеллы, определяющие расположение электронов в атоме.



