Гидрогалогенирование является одним из важных реакционных процессов в органической химии. Оно заключается в замещении атома водорода в органическом соединении атомом галогена, такими как хлор, бром или йод. Эта реакция широко используется в промышленности для получения органических галогенированных соединений, которые имеют широкий спектр применения в различных областях, включая лекарственную промышленность, сельское хозяйство и производство пластиков.
Одна из ключевых особенностей гидрогалогенирования заключается в том, что оно может приводить к нарушению правила Марковникова. Согласно правилу Марковникова, в присутствии кислородсодержащего соединения и неорганической кислоты, водород аддируется к углеводороду таким образом, чтобы образовывалась марковниковская продукт.
Однако в реакциях гидрогалогенирования можно наблюдать обратную ситуацию, когда атом галогена аддируется к углеводороду вместо водорода. Это нарушение правила Марковникова может происходить в определенных условиях, например, при наличии перекиси водорода или при использовании катализаторов. Такие реакции получили название анти-Марковниковских аддиций.
Влияние гидрогалогенирования на нарушение правила Марковникова
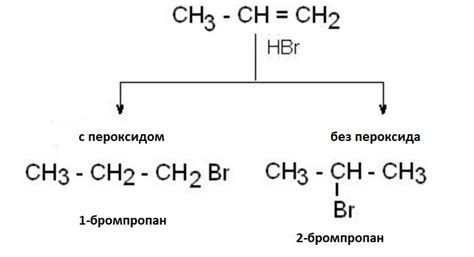
Однако, иногда в реакции гидрогалогенирования может происходить нарушение правила Марковникова, что означает, что галоген может добавляться к алкену таким образом, что он образует халогенид, в котором галоген занимает менее подвижное положение.
Нарушение правила Марковникова может происходить в следующих случаях:
- При наличии специфических катализаторов, которые могут изменить направление реакции.
- При высоких температурах или высоких концентрациях реагентов, которые могут привести к термической декомпозиции галогенида металла и изменению направления реакции.
- При наличии особенностей структуры алкена, например, наличии фенольных групп, которые могут стабилизировать промежуточные карбокатионы.
Нарушение правила Марковникова в гидрогалогенировании может привести к образованию различных продуктов и может играть важную роль в химической синтезе. Понимание причин и механизмов нарушения правила Марковникова является важным для развития новых методов синтеза органических соединений.
Процесс гидрогалогенирования
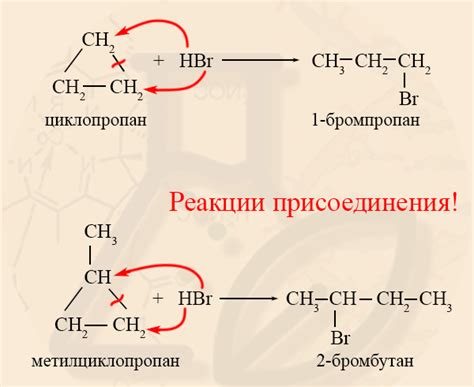
Одной из особенностей гидрогалогенирования является нарушение правила Марковникова. Согласно этому правилу, в результате электрофильного добавления водорода и галогена к алкену или алкину, водород присоединяется к углероду с наименьшим количеством водородных заместителей, а галоген к углероду с наибольшим. Однако, в реакции гидрогалогенирования может наблюдаться обратная ситуация, когда галоген присоединяется к углероду с наименьшим количеством заместителей.
Процесс гидрогалогенирования может протекать по двум различным механизмам: марковниковскому и анти-марковниковскому. В марковниковском механизме галоген присоединяется к углероду с наибольшим количеством заместителей, а в анти-марковниковском механизме - к углероду с наименьшим количеством заместителей.
Таблица ниже представляет сравнительное описание марковниковского и анти-марковниковского механизмов гидрогалогенирования.
| Марковниковский механизм | Анти-марковниковский механизм |
|---|---|
| Галоген присоединяется к углероду с наибольшим количеством заместителей | Галоген присоединяется к углероду с наименьшим количеством заместителей |
| Углерод с наименьшим количеством заместителей становится центральным атомом | Углерод с наибольшим количеством заместителей становится центральным атомом |
| Образуется более стабильное и малоактивное продукт | Образуется менее стабильное и активное продукт |
Правило Марковникова и его сущность

Правило Марковникова гласит, что при гидрогалогенировании (присоединении галогена и водорода) к двойной или тройной связи углерода, галоген будет присоединяться к углероду с большим числом заместителей, а водород - к углероду с меньшим числом заместителей. Иными словами, галоген придаст предпочтение более замещенному углероду, а водород - менее замещенному. Это означает, что галогенирование происходит с образованием наиболее стабильного карбокатиона.
| Вещество | Центральный углерод | Реакция |
|---|---|---|
| Этен | CH2=CH2 | HCl → CH3−CH2−Cl |
| Пропен | CH3−CH=CH2 | HBr → CH3−CH2−CH2−Br |
| 1-Бутилен | CH3−CH2−CH=CH2 | HCl → CH3−CH2−CH2−CH2−Cl |
Применение правила Марковникова позволяет предсказывать продукты реакции гидрогалогенирования и объяснить образование различных изомеров. Однако существуют исключения из правила Марковникова, когда гидрогалогенирование происходит по анти-Марковникову. Эти исключения связаны с наличием перекиси вещества или использованием особых катализаторов. В таких случаях правила Марковникова может быть нарушено, и галоген будет присоединяться к менее замещенному углероду.
Исключения из правила Марковникова

Вот некоторые примеры исключений из правила Марковникова:
- Галогенирование ацетилена: При галогенировании ацетилена, которое происходит в присутствии хлора или брома, атомы галогена добавляются к обоим углеродам ацетилена равномерно, создавая дихлорэтан или дибромэтан соответственно.
- Гидрогалогенирование алкенов с метиловой группой: В случае, если алкен содержит метиловую (CH3) группу, альтернативная реакция может произойти, и атомы галогена добавятся к углероду с метиловой группой вместо более замещенного углерода. Например, при гидрогалогенировании пропена с хлором, можно получить 2-хлорпропан вместо 1-хлорпропана.
Эти исключения можно объяснить с помощью различных факторов, таких как электронная плотность и геометрия молекулы. При ацетилене, двойная связь между углеродами обладает особой структурой, которая позволяет обоим углеродам участвовать в реакции галогенирования. В случае алкенов с метиловой группой, электронная плотность в метиловой группе может привлекать атом галогена.
Таким образом, правило Марковникова имеет исключения, при которых атомы галогена могут добавляться к менее замещенному углероду. Эти исключения являются важными особенностями процесса гидрогалогенирования и требуют дополнительного объяснения и изучения.
Нарушение правила Марковникова при гидрогалогенировании

Однако, существуют случаи, когда происходит нарушение правила Марковникова. Это происходит, когда реагенты обладают определенными свойствами или при определенных условиях. Нарушение правила Марковникова может происходить как при гидрогалогенировании, так и при других реакциях.
Одной из причин нарушения правила Марковникова является использование перекисей, таких как перекись водорода или перекись пероксикарбоновой кислоты, как источников галогенов. Использование перекисей может привести к образованию пероксидных связей с малозамещенными атомами водорода, что приводит к обратному по отношению к правилу Марковникова распределению галогена.
Другой причиной нарушения правила Марковникова является использование реагентов, обладающих электронными свойствами. Например, при гидрогалогенировании энолатов или аминоалканов, протекающем в присутствии галогенида меди(II), наблюдается нарушение правила Марковникова из-за образования комплексов меди с этикеткой отрицательного сурьмы.
| Примеры реакций с нарушением правила Марковникова: |
|---|
| Гидрогалогенирование алкенов с галогенидами ртения: |
| алкен + HBr → алкилгалоген + галогид ртения |
| Гидрогалогенирование алкенов с галогенидами бора: |
| алкен + HBr → алкилгалоген + галогид бора |
Нарушение правила Марковникова в гидрогалогенировании может иметь важное значение в синтезе органических соединений с определенными свойствами. Оно позволяет получать целевые продукты, которые не могли бы быть получены в рамках правила Марковникова. Поэтому изучение и понимание нарушения правила Марковникова имеет значительное практическое значение в химической промышленности и научных исследованиях.
Практическое применение нарушения правила Марковникова

Однако в некоторых случаях может происходить нарушение правила Марковникова, когда галоген атом присоединяется к углероду с меньшим числом атомов водорода. Это явление называется гидрогалогенированием и может иметь важное практическое применение в синтезе органических соединений.
Одним из примеров практического применения нарушения правила Марковникова является синтез ряда лекарственных препаратов. Например, при синтезе антигистаминных препаратов галоген атом может присоединяться к углероду с меньшим числом атомов водорода, что может значительно улучшить фармакологические свойства синтезируемого соединения.
Также нарушение правила Марковникова может быть использовано при синтезе пластичных полимеров. Некоторые полимеры, такие как полиэтилен с высокой плотностью (ПВД), могут быть получены благодаря гидрогалогенированию в условиях, когда галоген атом присоединяется к углероду с меньшим числом атомов водорода. Это позволяет получить полимеры с жесткой структурой и высокой плотностью, которые имеют широкое применение в промышленности.
Таким образом, нарушение правила Марковникова может быть полезным инструментом в органическом синтезе и поиске новых соединений с улучшенными свойствами. Практическое применение этого явления может способствовать развитию фармацевтической и химической промышленности, а также приносить пользу в других областях промышленности и научных исследований.



