Орбитали - это области пространства, в которых существует наибольшая вероятность нахождения электрона в атоме. Обычно мы представляем орбитали как трехмерные фигуры, такие как сферы или овалы, которые окружают ядро атома. Однако, существуют ли орбитали, которые могут существовать только в одномерном пространстве?
Одномерные орбитали, или орбитали 1d, представляют собой абстрактные математические модели, которые описывают поведение электрона в одной координатной оси. В отличие от трехмерных орбиталей, орбитали 1d нельзя визуализировать в привычном смысле - они существуют только на бумаге.
Орбитали 1d могут быть положительными, отрицательными или нейтральными, в зависимости от математической функции, которая описывает вероятность нахождения электрона в конкретной точке вдоль оси. Они играют важную роль в квантовой механике и помогают нам понять поведение электронов в узких наноструктурах или кристаллах.
Таким образом, орбитали 1d - это отличный инструмент для изучения и понимания поведения электронов в системах с ограниченной геометрией. Они позволяют нам более глубоко погрузиться в фундаментальные принципы квантовой механики и улучшить наше понимание взаимодействия атомов и молекул.
Может ли существовать 1D орбиталь?

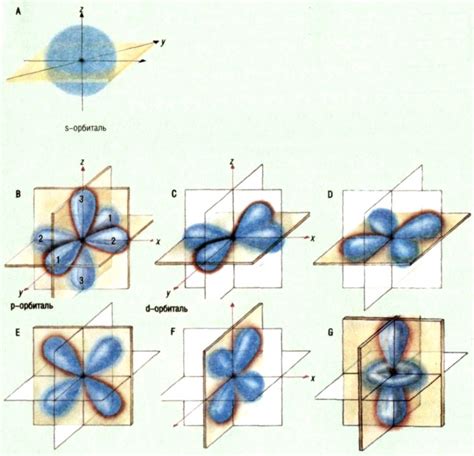
Орбитали могут иметь различные формы и размеры. Например, угловая орбиталь имеет форму шара, плоская орбиталь – форму прямоугольника, а орбиталь d-типа асимметричную форму с дополнительными lобовыми узлами.
Однако понятие 1D (одномерной) орбитали не имеет физического смысла. В трехмерном пространстве существуют только 2D и 3D орбитали, так как они имеют три координаты – x, y и z, чтобы полностью охватить все направления в пространстве.
Таким образом, понятие 1D орбитали противоречит трехмерной природе орбиталей и не имеет реальной физической основы.
| Вид орбитали | Форма |
|---|---|
| 1s | Сферическая |
| 2p | Плоская |
| 3d | Асимметричная с дополнительными лобовыми узлами |
Описание дискретной орбитали первого уровня
Орбиталь первого уровня может принять максимальное число двух электронов. Эти электроны обладают наименьшей энергией в атоме и называются электронами 1s. Они находятся в наиболее плотной и стабильной области пространства вокруг ядра атома.
Дискретная орбиталь первого уровня представляет собой точку, в которой находится электрон с наиболее низкой энергией в атоме. Она характеризуется квантовыми числами n = 1 (главное квантовое число) и l = 0 (момент импульса).
Орбиталь первого уровня играет важную роль в формировании электронной структуры атома и его химических свойств. Она определяет основные характеристики атома, такие как его радиус, массу и заряд.
Дискретная орбиталь первого уровня можно представить с помощью модели атома Бора или модели электронного облака, где электрон находится в определенной области пространства с высокой вероятностью.



