Реакции ионного обмена являются важным и распространенным физико-химическим процессом, который происходит между ионами различных веществ. Одним из интересных аспектов таких реакций является их способность образовывать газовые продукты. Газы, полученные в результате этих реакций, играют ключевую роль во многих отраслях науки и промышленности.
Образование газовых продуктов в процессе ионного обмена осуществляется за счет реакций, которые могут происходить как в водных растворах, так и в твердых веществах. В первом случае ионный обмен может приводить к выделению газовых продуктов в виде пузырьков, видимых невооруженным глазом. Во втором случае газ может образовываться внутри структуры твердого вещества и высвобождаться при нагревании, атмосферном давлении или при воздействии других условий.
Изучение реакций ионного обмена, приводящих к образованию газовых продуктов, имеет важное значение во многих научных областях. Оно позволяет понять, как происходят химические реакции в растворах и твердых веществах, какие вещества обладают свойствами газообразного состояния, и какие факторы влияют на скорости ионного обмена и образования газовых продуктов.
Реакции ионного обмена в процессе формирования газовых продуктов

Одной из наиболее распространенных реакций ионного обмена, приводящей к образованию газовых продуктов, является реакция между кислотами и основаниями. Например, при взаимодействии соляной кислоты и гидроксида натрия образуется натриевая соль и вода. В данном случае, образование натриевой соли сопровождается выделением молекулы газа – воды.
| Реакция | Ионный обмен | Газовый продукт |
|---|---|---|
| Соляная кислота + Гидроксид натрия → Натриевая соль + Вода | H+ + Cl- + Na+ + OH- → Na+ + Cl- + H2O | H2O |
В данном примере, кислотный и ионный компоненты реагируют, образуя натриевую соль и воду. Вода, являющаяся жидкой на комнатной температуре, при такой реакции выделяется в виде газа благодаря тому, что реакция происходит водным растворе.
Такие реакции широко применяются в различных отраслях промышленности. Например, в химическом производстве они используются для получения определенных газов, таких как водород или карбонат водорода. Кроме того, ионный обмен играет важную роль в обработке воды и сточных вод, позволяя удалить излишки солей и тяжелых металлов.
Таким образом, реакции ионного обмена в процессе формирования газовых продуктов играют важную роль в различных областях нашей жизни. Они позволяют получать необходимые газы для промышленности, а также обрабатывать и очищать воду. Изучение ионного обмена и его реакций помогает разработать более эффективные методы производства и очистки, что в свою очередь положительно влияет на экологию и качество жизни людей.
Механизм реакций ионного обмена
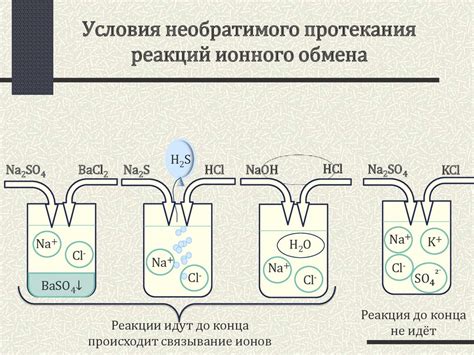
Основным механизмом реакций ионного обмена является обмен ионами между двумя различными ионами или ионами и веществом. Этот процесс может происходить как в растворах, так и в твердом состоянии.
Реакции ионного обмена в растворах происходят, когда ионы одного вещества замещают ионы другого вещества. Это может происходить в результате диссоциации веществ в растворе или при взаимодействии двух различных растворов.
| Примеры реакций ионного обмена | Уравнение реакции |
|---|---|
| Образование осадка | A2+ + B- → AB |
| Образование кислоты | OH- + H+ → H2O |
| Образование соли | Na+ + Cl- → NaCl |
В твердом состоянии реакции ионного обмена могут происходить при взаимодействии двух различных твердых веществ. В таких случаях ионы одного вещества замещают ионы другого вещества в кристаллической решетке.
Механизм реакции ионного обмена в твердых фазах зависит от типа ионной связи, особенностей кристаллической решетки и энергии активации реакции. Эти факторы определяют скорость и направление реакции ионного обмена в твердом состоянии.
Реакции ионного обмена играют важную роль в различных химических процессах, таких как образование солей, кислот и осадков. Изучение механизма этих реакций позволяет более глубоко понять процессы, происходящие в химических системах и использовать полученные знания для создания новых материалов и технологий.
Влияние ионного обмена на образование газовых продуктов

Например, рассмотрим реакцию между раствором соли NaCl и кислотой HCl. При смешивании этих растворов происходит ионный обмен, при котором ионы Na+ из раствора соли замещают ионы H+ из кислоты. Таким образом, образуются два продукта: раствор соли NaCl и раствор кислоты HCl.
В некоторых случаях при ионном обмене могут образовываться газовые продукты. Например, рассмотрим реакцию между раствором соли Na2CO3 и кислотой HCl. При смешивании этих растворов происходит ионный обмен, при котором ионы Na+ из раствора соли замещают ионы H+ из кислоты. В результате образуется раствор NaCl, а также образуется газ CO2. Образование газа CO2 возникает из-за того, что карбонатные ионы CO32- в растворе соли реагируют с ионами H+ из кислоты, образуя H2O и CO2.
Таким образом, ионный обмен может приводить к образованию газовых продуктов в химических реакциях. Это явление имеет большое значение в различных областях, включая промышленность, экологию и биологию.
Примеры реакций ионного обмена с образованием газовых продуктов

Один из примеров реакции ионного обмена с образованием газовых продуктов - реакция между карбонатом натрия (Na2CO3) и сульфатом меди (CuSO4). При смешивании этих веществ в растворе образуется газ диоксид углерода (CO2), который можно наблюдать в виде пузырьков, поднимающихся вверх.
Na2CO3 + CuSO4 → Na2SO4 + CuCO3
CuCO3 → CuO + CO2
Другим примером является реакция между хлоридом натрия (NaCl) и серной кислотой (H2SO4). При смешивании этих веществ в растворе образуется газ хлороводород (HCl), который обладает резким запахом. В этом случае, газ виден в виде облачка и возможно появление белой дымки.
NaCl + H2SO4 → NaHSO4 + HCl
Реакции ионного обмена с образованием газовых продуктов широко применяются в промышленности и лабораторной практике. Они играют важную роль в многих процессах, таких как десульфурация газов, очистка воды и производство химических соединений.



