Реакция магния с соляной кислотой является одной из наиболее известных химических реакций. Эта реакция хорошо изучена и широко применяется в химических лабораториях и промышленности. Магний - это металл, который обладает множеством полезных свойств и применяется в различных сферах.
Основным компонентом реакции является соляная кислота, которая представляет собой сильное кислотное соединение. В химической реакции, магний и соляная кислота взаимодействуют, образуя хлорид магния и выделяя водород. Это одна из эндотермических реакций, то есть реакция, в процессе которой поглощается энергия.
Реакция магния с соляной кислотой происходит при определенных условиях. Во-первых, требуется наличие соляной кислоты концентрацией выше 3%, иначе реакция может протекать неполносью или быть слишком медленной. Во-вторых, магний должен быть в достаточно чистом состоянии, без оксидной пленки на поверхности, чтобы реакция проходила эффективно. В-третьих, желательно проводить реакцию в условиях отрицательного давления, чтобы ускорить скорость реакции и увеличить выход продукта.
Реакция магния с соляной кислотой может быть использована для получения хлорида магния, который также имеет широкое применение. Хлорид магния используется в производстве лекарств, пищевой промышленности, в сельском хозяйстве и других отраслях. Кроме того, эта реакция может быть использована в качестве учебного эксперимента, чтобы показать студентам принципы химических реакций и ознакомить их с основными свойствами магния и соляной кислоты.
Условия и реакционная способность магния
Однако, для успешной реакции магния с соляной кислотой необходимо соблюдение определенного набора условий. Во-первых, оба реагента должны находиться в жидком состоянии. Для этого магний может быть предварительно подготовлен в виде металлической стружки или порошка, а соляная кислота должна быть взята в концентрированном состоянии.
Во-вторых, важным условием реакции является наличие катализатора. В большинстве случаев в качестве катализатора используется платиновая проволока или графитовая стержень. Катализатор ускоряет реакцию между магнием и соляной кислотой, повышая ее скорость.
Также, еще одним условием реакции является температура. Реакция магния с соляной кислотой протекает при повышенных температурах, обычно в пределах 70-90 градусов Цельсия. Высокая температура способствует активации молекул, что способствует более быстрой реакции.
Таким образом, условия и реакционная способность магния при взаимодействии с соляной кислотой тесно связаны друг с другом. Соблюдение определенных условий, таких как наличие жидких реагентов, использование катализатора и заданной температуры, позволяет достичь оптимального результата в виде успешной и скоростной реакции между магнием и соляной кислотой.
Основные характеристики соляной кислоты

Соляная кислота является сильным одноэлектронным кислородсодержащим кислотным соединением. Она обладает еще несколькими характеристиками:
1. Кислотные свойства: соляная кислота способна отдавать протон (H+) воде или другим основаниям, образуя соли.
2. Высокая степень диссоциации: в водных растворах она полностью диссоциирует на ионы водорода и ионы хлорида. Это позволяет быстро и полностью реагировать с другими веществами.
3. Сильное коррозийное действие: соляная кислота обладает высокой агрессивностью и может разрушать различные материалы, включая металлы и органические вещества.
4. Низкий pH: соляная кислота является кислотным раствором с очень низким значением pH, что обусловлено большим количеством протонов (H+) в растворе.
5. Однако, не смотря на ее агрессивность, она широко используется в различных промышленных процессах, в производстве удобрений, фармацевтической и косметической промышленности в качестве необходимого реагента.
Механизм реакции между магнием и соляной кислотой
1. Сначала происходит протекание двух параллельных реакций:
Магний (Mg) + 2H2O ⇆ Mg(OH)2 + H2 (Реакция 1)
Соляная кислота (HCl) + H2O ⇆ H3O+ + Cl- (Реакция 2)
2. Реакция 1 приводит к образованию гидроксида магния и выделению молекул водорода.
3. Реакция 2 образует ион водорода и анион хлорида. Анион хлорида диссоциирует на ионы хлорида и протон в водной среде.
4. Ионы хлорида вступают в реакцию с гидроксидом магния:
Mg(OH)2 + 2Cl- ⇆ MgCl2 + 2OH- (Реакция 3)
5. Таким образом, ионы хлорида реагируют с гидроксидом магния, образуя магниевую соль и гидроксид.
Итоговое уравнение реакции можно представить следующим образом:
Mg + 2HCl ⇆ MgCl2 + H2
Таким образом, механизм реакции между магнием и соляной кислотой включает образование ионов водорода и цепочку превращений магния и хлорида. Эта реакция является типичным примером активного металла, реагирующего с кислотой и образующего соль и водород.
Процесс действия соляной кислоты на магний

Соляная кислота (HCl) является достаточно сильным кислотным веществом, поэтому при взаимодействии с магнием происходит активное образование гидрохлоридов. Реакция протекает в два этапа:
1. Образование хлорида магния (MgCl2):
2HCl + Mg → MgCl2 + H2
В данной реакции две молекулы соляной кислоты взаимодействуют с одной молекулой магния, образуя одну молекулу хлорида магния и выделяя молекулу водорода.
2. Выделение молекулы водорода:
2HCl + Mg → MgCl2 + H2
Водород является природным продуктом данной реакции и образуется в результате цепочки химических превращений. Он является газообразным веществом и выделяется во время реакции в виде пузырьков.
Обратите внимание: Реакция магния с соляной кислотой является сильной экзотермической реакцией, что означает, что сопровождается выделением тепла. Поэтому реакция может сопровождаться появлением паров и дыма, а также суммарным увеличением объема смеси веществ.
Зависимость скорости реакции от условий
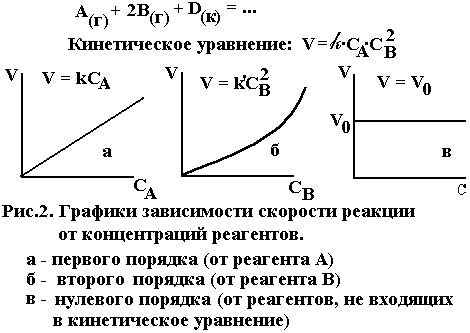
Скорость реакции между магнием и соляной кислотой может зависеть от нескольких условий, включая температуру, концентрацию реагентов и поверхность контакта.
Температура играет ключевую роль в определении скорости реакции. При повышении температуры молекулы обладают большей энергией, что способствует частым и успешным столкновениям между реагентами, и, соответственно, увеличивает скорость реакции. Наоборот, при низкой температуре молекулы движутся медленно, что снижает скорость реакции.
Концентрация реагентов также влияет на скорость реакции. Повышение концентрации реагентов увеличивает вероятность столкновения между ними, что приводит к повышению скорости реакции. В то же время, уменьшение концентрации реагентов снижает вероятность успешных столкновений и, следовательно, снижает скорость реакции.
Поверхность контакта также оказывает влияние на скорость реакции. Чем больше поверхность магния, на которую может воздействовать соляная кислота, тем больше активных участков для реакции. Повышение поверхности магния (например, путем дробления магниевой пластинки на мелкие частицы) увеличивает количество активных участков, что ускоряет реакцию между магнием и соляной кислотой.



