Оксиды – это химические соединения, состоящие из атомов кислорода, связанных с атомами других элементов. Оксиды находят широкое применение в различных отраслях науки и промышленности. Одной из ключевых реакций, связанных с оксидами, является реакция с кислотами.
Кислоты – это вещества, обладающие кислотностью и способные отдавать водородные ионы (H+) в реакциях с другими веществами. Реакция кислоты с оксидом носит название оксидационно-восстановительной реакции и происходит в следующем порядке.
Сначала оксид разлагается под влиянием кислотного раствора, образуя ион гидроксида и ион кислоты. Второй этап реакции – образование воды. При этом ион H+ вступает в реакцию с ионом OH-, образуя молекулу воды. В результате реакции образуются вещества, которые являются основными компонентами оксида и кислоты.
Взаимодействие кислот и оксидов

Во время реакции кислота отдает протон (водородный ион), а оксид получает этот протон. В результате образуется соль и вода. Такой тип реакции называется кислотно-основным взаимодействием. Например, когда серная кислота (H2SO4) реагирует с оксидом меди (CuO), образуется соль меди (CuSO4) и вода (H2O.
Реакция кислоты с оксидом может также называться нейтрализацией, так как образовавшаяся соль обладает нейтральным pH. Кроме того, процесс взаимодействия кислоты и оксида может сопровождаться выделением тепла и образованием пены или газовых пузырей.
Важно отметить, что разные кислоты могут реагировать с оксидами по-разному. Некоторые оксиды могут образовывать не только соли, но и дополнительные продукты реакции, такие как перекиси. Поэтому взаимодействие кислот и оксидов является сложным процессом, требующим детального изучения и анализа.
Процесс химической реакции
Процесс реакции начинается с взаимодействия между ионами кислоты и ионами оксида. Ионы кислоты обычно содержат водород, который высвобождается при контакте с оксидом. В результате происходит протекание протолитической реакции, в ходе которой ионы водорода и ионы оксида обмениваются местами.
Для запуска реакции требуется наличие веществ, способных взаимодействовать между собой. Такими веществами могут быть кислоты, содержащие в своем составе кислород, и оксиды, в состав которых входят металлы или неметаллы. Именно взаимодействие этих веществ и обуславливает процесс химической реакции.
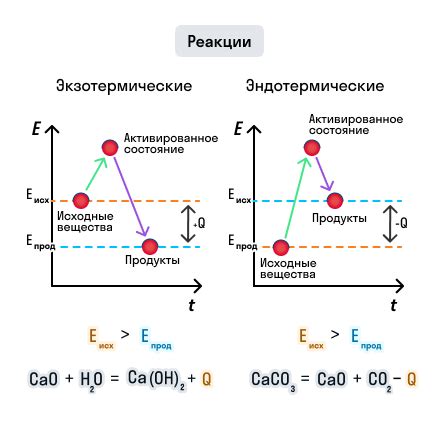
Процесс реакции между кислотой и оксидом может сопровождаться выделением тепла или света. В таких случаях реакция называется экзотермической. Однако, могут существовать и эндотермические реакции, во время которых поглощается тепло. Они могут происходить, если реакция требует большей энергии для протекания.
Окончательный продукт химической реакции является солью и водой. Вода образуется в результате соединения водородных и оксидных ионов, а соль получается путем соединения ионов кислоты и ионов оксида. Конечные продукты реакции определяются исходными веществами, принимающими в ней участие.
Таким образом, процесс реакции кислоты с оксидами представляет собой важный этап в химии, где происходит переход веществ из одного состояния в другое. Этот процесс имеет большое значение как в лабораторных условиях, так и в промышленности, где используется для производства различных химических соединений.
Образование солей и воды

Реакция кислоты с оксидами приводит к образованию солей и воды. Соли образуются в результате нейтрализации кислоты и основания, при этом от оксида отщепляются кислородные атомы, которые сливаются с водой, образуя молекулы воды. Образовавшиеся вещества в данной реакции называются солями.
Процесс образования солей и воды может быть иллюстрирован с помощью таблицы:
| Кислота | Оксид | Соль | Вода |
|---|---|---|---|
| Серная кислота | Оксид серы VI | Сульфат | Вода |
| Азотная кислота | Оксид азота V | Нитрат | Вода |
| Уксусная кислота | Оксид углерода IV | Ацетат | Вода |
Таким образом, реакция кислоты с оксидами приводит к образованию солей и воды, что является важным химическим процессом с точки зрения многих промышленных и научных приложений.
Роль оксидов в химических реакциях
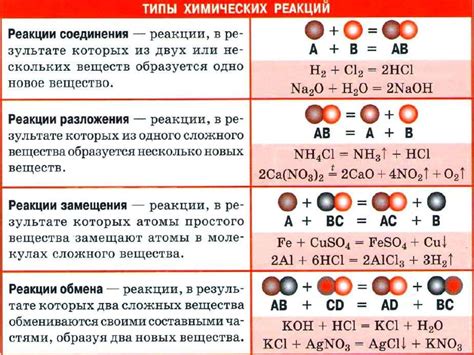
Реакция оксида с водой порождает либо кислотное, либо щелочное решение. Если оксид является основой, он будет реагировать с водой, образуя щелочь, например:
- Оксид натрия (Na2O) + вода (H2O) → щелочь NaOH
- Оксид калия (K2O) + вода (H2O) → щелочь KOH
Если оксид является кислотным, реакция с водой приведет к образованию кислоты, например:
- Оксид серы (SO2) + вода (H2O) → серная кислота (H2SO4)
- Оксид углерода (CO2) + вода (H2O) → угольная кислота (H2CO3)
Таким образом, оксиды являются важными компонентами химических реакций, так как они могут образовывать основы или кислоты, зависимо от их химических свойств. Это позволяет использовать оксиды для контроля pH растворов и поддержания оптимальных условий для различных процессов.



